Page 1 - nmCRPC Clinical Support Tool-MARCH2021
P. 1
Traitement du CPRC non métastatique
TRAITEMENTS CIBLANT LES RA
Traitement du CPRC non métastatique – TRAITEMENTS CIBLANT LES RA
Trois agents ciblant les récepteurs des androgènes (RA) ont été approuvés au Canada pour le traitement du
cancer de la prostate résistant à la castration et non métastatique (CPRCnm) – soit l’apalutamide, le darolutamide
et l’enzalutamide. Ces traitements peuvent être prescrits aux patients ayant reçu un diagnostic de CPRCnm à
risque élevé ayant les caractéristiques suivantes :
• Temps de doublement de Aperçu des essais de phase III sur le CPRCnm
l’antigène prostatique spécifique SPARTAN 1,2 ARAMIS 3 PROSPER 4
(TDAPS) ≤ 10 mois Apalutamide vs Darolutamide vs Enzalutamide vs
Traitement
• TDM et scintigraphie osseuse ne placebo placebo placebo
révélant aucun signe de métastases Taille de 1207 1509 1401
• Taux de testostérone correspondant l’échantillon
aux taux après castration Principal SSM (intervalle avant l’apparition de métastases ou le décès)
critère
( < 1,7 nmol/L) d’évaluation
Les essais cliniques de phase III portant Critère CPRCnm avec APS > 2 ng/mL et TDAPS ≤ 10 mois
sur chacun des trois traitements ciblant d’admissibilité
les RA avaient des critères d’inclusion Critères Antécédents de crises Antécédents de crises
convulsives ou
convulsives ou
similaires, et ont présenté des résultats d’exclusion de toute maladie Aucun de toute maladie
liés à des
positifs similaires quant au principal maladies pouvant prédisposer pouvant prédisposer
critère d’évaluation, soit la survie sans neurologiques aux crises convulsives aux crises convulsives
métastase (SSM). Tous les patients ont continué à recevoir un traitement par privation androgénique
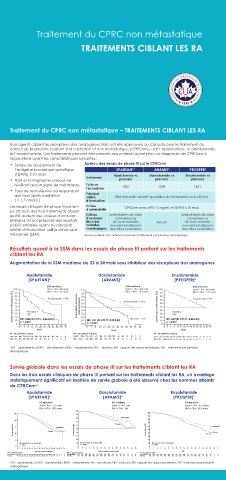
Résultats quant à la SSM dans les essais de phase III portant sur les traitements
ciblant les RA
nmCRPC Phase 3 Tr
nmCRPC Phase 3 Trials: Primary Endpoint –MFSnmCRPC Phase 3 Trials: Primary Endpoint –MFSials: Primary Endpoint –MFS
nmCRPC Phase 3 Trials: Primary Endpoint – MFSTrials: Primary Endpoint – MFSnmCRPC Phase 3 Trials: Primary Endpoint – MFS
nmCRPC Phase 3
Augmentation de la SSM médiane de 22 à 24 mois sous inhibiteur des récepteurs des androgènes
Darolutamide
Apalutamide
Apalutamide Enzalutamide Enzalutamide Darolutamide Darolutamide
Enzalutamide
Apalutamide
Darolutamide
Apalutamide
Enzalutamide
(PROSPER)
(SPARTAN)
(SPARTAN) 2 (PROSPER) 2 2 3 (PROSPER) 3 4 2 (ARAMIS) 4 3 4 (ARAMIS) 4
(SPARTAN)
(ARAMIS)
(SPARTAN)
(PROSPER)
(ARAMIS) 3
SSM médiane
SSM médiane 100 SSM médiane 100 100 SSM médiane 1.0 100 SSM médiane 1.0 SSM médiane
SSM médiane
SSM médiane
Median MFS
Median MFS
Median MFS
Median MFS Median MFS
Median MFS
SSM médiane
Median MFS
Median MFS
Median MFS
APA + TPA : 40,5 mois
APA + TPA : 40,5 mois
DARO + TPA : 40,4 mois
DARO + TPA : 40,4 mois
APA + TPA : 40,5 mois
DARO + TPA : 40,4 mois
100
ENZA + TPA : 36,6 mois
100
ENZA + TPA : 36,6 mois
ENZA + TPA : 36,6 mois
DARO + ADT: 40.4 mo
DARO + ADT: 40.4 mo
Survie sans métastase (%) 100 Placebo + Apalutamide + TPA Survie sans métastase (%) 100 Placebo + Apalutamide + TPA Probabilité de survie Metastasis-free survival Survie sans métastase (%) 1.0 Survie sans métastase (%) 100 TPA Enzalutamide + TPA Probabilité de survie l Metastasis-free surviva sans métastase probability 0.8 Survie sans métastase (%) 100 Placebo + Darolutamide + TPA Probabilité de survie Metastasis-free survival sans métastase probability 0.8
APA + ADT: 40.5 mo
ENZA + ADT: 36.6 mo 40.5 mo
DARO + ADT: 40.4 mo
APA + ADT:
APA + ADT: 40.5 mo
ENZA + ADT: 36.6 mo
ENZA + ADT: 36.6 mo
100
Survie sans métastase (%) 100
PBO + TPA : 18,4 mois 1.0
1.0
1.0
PBO + TPA : 18,4 mois
PBO + TPA : 18,4 mois
PBO + TPA : 16,2 mois
PBO + TPA : 16,2 mois
PBO + TPA : 16,2 mois
PBO + TPA : 14,7 mois
PBO + TPA : 14,7 mois
PBO + ADT:
PBO + ADT: 16.2 mo
PBO + TPA : 14,7 mois 18.4 mo
90
PBO + ADT: 16.2 mo
PBO + ADT:
PBO + ADT: 18.4 mo
90
PBO + ADT: 14.7 mos 16.2 mo
PBO + ADT: 18.4 mo
90
90
0.9
PBO + ADT: 14.7 mos
PBO + ADT: 14.7 mos
0.9
90 90
0.9
90
Metastasis-free survival (%)
Metastasis-free survival (%)
Metastasis-free survival (%)
90
Metastasis-free survival (%)
Metastasis-free survival (%)
90
Metastasis-free survival (%)
90 90
90 0.9
0.9
0.9
80
80
0.8
80
80 80
80
80
80
80 80
80
0.8
80 0.8
0.8
sans métastase
Apalutamide + TPA
Enzalutamide + TPA
Enzalutamide + TPA
70
70
Enzalutamide + ADT
Apalutamide + ADT
Apalutamide + ADT
Enzalutamide + ADT
Enzalutamide + ADT
70
70 70
Apalutamide + ADT
70
0.7
0.7
0.7
70
70
70 0.7
70 70
0.7
probability
70
Darolutamide + TPA 0.7
Darolutamide + ADT
Darolutamide + ADT
Darolutamide + ADT
60
60
60
60 60
60
0.6
0.6
0.6
60
60
60 60
0.6
0.6
60 0.6
60
50
50
50
50
50 50
0.5
0.5
0.5
50
0.5
50
50 0.5
0.5
50
50 50
0.4
0.4
40
0.4
40
40
40 40
40
40
0.4
0.4
40
40 40
40 0.4
40
Placebo +
Placebo + Placebo +
Placebo +
Placebo + Placebo +
Placebo +
Placebo +
Placebo +
0.3
0.3
30
30
0.3
30
30 30
30
30
0.3
30 30
TPA
0.3
TPA
30 0.3
30
TPA
TPA
TPA
30
ADT
ADT
ADT
ADT
ADT
ADT
0.2
20
20
20
20
20
20
0.2
20 0.2
20 20
20
RRI : 0,28 (IC à 95 % : 0,23-0,35)
RRI : 0,29 (IC à 95 % : 0,24-0,35)
RRI : 0,29 (IC à 95 % : 0,24-0,35)
RRI : 0,29 (IC à 95 % : 0,24-0,35)
RRI : 0,28 (IC à 95 % : 0,23-0,35) Placebo + ADT
HR 0.29 (95% CI 0.24–0.35)
HR 0.28 (95% Cl 0.23–0.35)
Placebo + ADT
HR 0.28 (95% Cl 0.23–0.35)
HR 0.29 (95% CI 0.24–0.35)
10 10 HR 0.28 (95% Cl 0.23–0.35)
Placebo + ADT
HR 0.29 (95% CI 0.24–0.35)
0.1
0.1
0.1
10
10
10
10
HR 0.41 (95% CI 0.34–0.50)
HR 0.41 (95% CI 0.34–0.50)
HR 0.41 (95% CI 0.34–0.50)
10
10 0.1
0.1
10
0.1
10
10 10
p < 0,001
p < 0,001
p < 0,001
p < 0,001
p < 0,001 p < 0,001
p < 0.001
p < 0.001
p < 0.001
p < 0.001
p < 0,001 p < 0.001
p < 0,001
p < 0,001
0 0 RRI : 0,28 (IC à 95 % : 0,23-0,35) 20 20 p < 0.001 0.2 RRI : 0,41 (IC à 95 % : 0,34-0,50) Placebo + TPA 0.2 RRI : 0,41 (IC à 95 % : 0,34-0,50) Placebo + TPA 0.2 RRI : 0,41 (IC à 95 % : 0,34-0,50) Placebo + TPA
0.0
0.0
p < 0.001
0
p < 0.001
p < 0.001
0.0
0 0
0
0 0.0
0.0
0.0
0
0
00
0
21 24 27
8 12 16 20 24 24 27
30 33 36 3942
36 9 12 15 18
30 33 36
21 24
4
8
0 0 4 4 8 12 16 20 24 28 32 36 40 44 0 0 0 0 4 36 9 12 15 18 21 28 32 36 40 44 0 0 3 6 9 12 15 180 0 36 9 12 15 18 8 12 16 20 240 121620 24 28 32 36 39 42 44 4836 2816 20 240 12 16 20 24 30 33 36 3942 36 40 44 0 0 4 4 8 0 0 121620 24 28 32 36 27 40 44 48 3942 0 0 4 4 8 8 121620 24 28 32 36 40 44 48
4
30 33 36
40 32 36 40
30 33 36
8
21
12 16 20 24 28 32 36
28 32 36 40 44
8 12 16 20 24
28 32 36 40 44 42
30 33 36 39
40
28 32 44 48 44
21 24
3 6 9 12 15 18
40 44 48
4 3 6 9 12 15 18
8 12
4
21 24 27 28 32
12 16 20 24 28 32 36 27
8
40 44 48 39 42
8 12 16 20 2424 27
4
Mois Mois Mois Mois Months Mois Mois Mois
Mois
Mois
Months
Months
Months
Months
Months Months
N bre à risque à risque
N bre à risque
N bre à risque
N bre à risque No. at risk N bre à risque N bre à risque N bre à risque No. at risk Months N bre à risque Months
N bre
No. at risk
No. at risk
N bre de patients à risque
N bre de patients à risque
No. at risk
No. at risk
No. at risk
No. at risk
N bre de patients à risque
No. at risk
506
68
/,+ /+' ,.' -+/ 189262377
675
37
675
, 0
345!#$ !%&0,, ')- !"!#$!%& '()506
,0' 116
** +'(
!"!#$!%& '() *+, )-. -+/ ,0' .'. +'( 0) ,) 36 +) 16 , 3 ( 0 345!#$ !%&0,, 806 865 759 637 528 431 418 328 237 0) +-0 '* 36 ** 16 , / ( ( 0 0 DARO + TPA 955 817 *-0 ),* -.' 506713 652 514 398 282 180 96 / 4 ( ,) 18 0 18 36 +) 2 2 16 DARO + ADT 955 817 !%&0,, ')- *-0 262 -.' 189 431 418 328 68 .,* 37 159 18 ** 2 31 0 / ( 0 DARO + TPA 955 817 675 506 377 262 189 116 68 68 37 37 18 18 2 2 0 0
.'.
+-0 '* .'.
-+/
,)
*+, )-.
(
68
262
116
377
189
506
.,* 189
377
116
262
377
116
+'( .,*
/,+
*-0
,0' /+' ,.'
DARO + TPA
506
*+, )-. ),* -.'
675
189 /,+ /+'
,+ 0) 37
345!#$ 675817
955 817
DARO + ADT
0
APA + ADT 806 713 652 514 398 282 180 96
675 806
APA + ADT
0 3
955 817 ADT
APA +
DARO + ADT
DARO + TPA 955 ENZA + ADT 933 865 759 637
!"!#$!%& '() ')- 713 652 514 398 282 180 96 159 87 77 31
ENZA + ADT 933
APA + TPA
+) ,+ 3 4
ENZA + TPA
116 ,.' 68 237
377 ),* 262 528
2 ,+ 0 4
37 +-0 '* 18 87 77
ENZA + ADT 933 865 759 637 528 431 418 328 237 159 87 77 31
4
180
275
(
75
,/
-'
12
PB
0
.0+ 117
0
+-,
"12#$#!%& /(+ .0+ ..( +-, 0+ 91 -' 58 ,/ 34 +, 13 - 5 + 1 ( 0 ( 0 PBO + TPA .0+ ..( .+. +-* +(-0' 58 ,/ /0 13 - 5 + 1 5 ( + ( ( 0 0 PBO + TPA 554 368 .0) .+. +-* +(-0' ..( )/ +-, /0 0+ 2950 ,++)++- +, + 1 ( - 0 0 0 5 + 0 0 1 ( 0 0 0 PBO + TPA 554 368 275/)' /.( .0) 75 +-* 50 105 29 )/ 12 49 4,++)++- 0+ ( 0 PBO + TPA 554 368 275 180 117 75 75 50 50 29 29 12 12 4 4 0 0 0 0 0 0
"12#$!%& /)' /.( "12#$#!%& /(+ 180O + TPA
0+
+, ,++)++-
"12#$!%&
.0)
PBO + ADT 401 291 220 153
554 368
275
180
0
PBO + ADT
117
554 368
PBO + ADT
117
275 401
PBO + ADT
180
PBO + ADT
-' )/ 34
PBO + ADT 468 420 296 212 157 105 98 64 49 31 16 11 12295075117180291 220 153
91
0
5 4 13
91
58
34
275 468 420 296 212
PBO + TPA
PBO +
0 5
554 368 ADT
0 1
0 1
50 +(-0' 29 98 64
PBO + ADT 468
"12#$!%& /)' 401 420 296 212
PBO + ADT
117 .+. 75157
12 /0 4 31 16 11
"12#$#!%& /(+ /.( 291 220 153 157 105 98 64 49 31 16 11
APA = apalutamide; DARO = darolutamide; ENZA = enzalutamide; PBO = placebo; RRI = rapport des risques instantanés; TPA = traitement par privation
androgénique
ADT = Androgen deprivation therapy; APA = Apalutamide; ADT = Androgen deprivation therapy; APA = Apalutamide; 1. Smith MR ADT = Androgen deprivation therapy; APA = Apalutamide;, et al. N Engl J Med 2018;378:1408; 1. Smith MR, et al. N Engl J Med 2018;378:1408; 1. Smith MR, et al. N Engl J Med 2018;378:1408;
ADT = Androgen deprivation therapy; APA = Apalutamide;
2. Hussain M, et al. N Engl J Med 2018;378:2465; 3. Fizazi K, et al. N En
DARO = Darolutamide; ENZA = Enzalutamide; ADT = Androgen deprivation therapy; APA = Apalutamide; 1. Smith MR, et al. N Engl J Med 2018;378:1408; ADT = Androgen deprivation therapy; APA = Apalutamide 1. Smith MR, et al. N Engl J Med 2018;378:1408; ; 1. Smith MR, et al. N Engl J Med 2018;378:1408;
DARO = Darolutamide; ENZA = Enzalutamide;
2. Hussain M, et al. N Engl J Med 2018;378:2465; 3. Fizazi K, et al. N Engl J Med 2019;380:12352. Hussain M, et al. N Engl J Med 2018;378:2465; 3. Fizazi K, et al. N Engl J Med 2019;380:1235gl J Med 2019;380:1235
DARO = Darolutamide; ENZA = Enzalutamide;
DARO = Darolutamide; ENZA = Enzalutamide;
DARO = Darolutamide; ENZA = Enzalutamide;
DARO = Darolutamide; ENZA = Enzalutamide;
2. Hussain M, et al. N Engl J Med 2018;378:2465; 3. Fizazi K, et al. N Engl J Med 2019;380:1235l J Med 2019;380:1235
2. Hussain M, et al. N Engl J Med 2018;378:2465; 3. Fizazi K, et al. N Engl J Med 2019;380:1235
2. Hussain M, et al. N Engl J Med 2018;378:2465; 3. Fizazi K, et al. N Eng
HR = Hazard ratio; PBO = Placebo HR = Hazard ratio; PBO = Placebo HR = Hazard ratio; PBO = PlaceboSlide provided by Dr. Fred Saad Slide provided by Dr. Fred Saad Slide provided by Dr. Fred Saad
Slide provided by Dr. Fred Saad
HR = Hazard ratio; PBO = Placebo
Slide provided by Dr. Fred Saad
Slide provided by Dr. Fred Saad Hazard ratio; PBO = Placebo
HR =
HR = Hazard ratio; PBO = Placebo
Survie globale dans les essais de phase III sur les traitements ciblant les RA
Dans les trois essais cliniques de phase III portant sur les traitements ciblant les RA, un avantage
statistiquement significatif en matière de survie globale a été observé chez les hommes atteints
de CPRCnm 5-7
Apalutamide Darolutamide Enzalutamide
(SPARTAN) 5 (ARAMIS) 6 (PROSPER) 7
SG médiane SG médiane SG médiane
APA + TPA : 73,9 mois DARO + TPA : NA ENZA + TPA : 67,0 mois
PBO + TPA : 59,9 mois PBO + TPA : NA PBO + TPA : 56,3 mois
100
100
100
90
90
80 Darolutamide
80 80
70 60 Placebo 70
Survie globale (%) 60 40 Placebo Apalutamide Survie globale (%) 50 40 Survie globale (%) 60 50 40 Placebo Enzalutamide
20 30 20 30 20
RRI : 0,78 (IC à 95 % : 0,64–0,96) 10 RRI : 0,69 (IC à 95 % : 0,53–0,88) 10 RRI : 0,73 (IC à 95 % : 0,61–0,89)
p = 0,016 p = 0,003 p = 0,001
0 0 0
0 4 8 12 16 20 24 28 32 36 40 44 48 52 56 60 64 68 72 76 0 4 8 12 16 20 24 28 32 36 40 44 48 52 56 60 0 4 8 12 16 20 24 28 32 36 40 44 48 52 56 60 64 68 72
Mois après la randomization Mois depuis la randomisation Mois
N bre de patients à risque N bre de patients à risque N bre de patients à risque
Apalutamide 806 791 774 758 739 717 691 658 625 593 558 499 376 269 181 100 47 19 4 0 Darolutamide 955 932 908 863 816 771 680 549 425 293 214 129 69 37 12 0 Enzalutamide 933 926 910 897 874 850 822 782 700 608 517 424 327 244 169 89 33 4 0
Placebo 401 392 385 373 358 339 328 306 286 263 240 204 156 114 82 38 21 6 2 0 Placebo 554 530 497 460 432 394 333 261 182 130 93 54 28 16 4 0 Placebo 468 467 459 444 428 404 381 363 321 274 219 177 140 106 64 30 16 3 0
APA : apalutamide; DARO : darolutamide; ENZA : enzalutamide; NA : non atteint; PBO : placebo; RRI : rapport des risques instantanés; TPA : traitement par privation
androgénique